Как известно, вирусы — объекты странные: вроде, и не живые сами по себе, но стоит только попасть в клетку... Внутриклеточные подвиги бактериофагов описаны давно, однако эти вирусы сумели сохранить парочку секретов — настоящих жареных фактов, по меркам научной периодики. Например, в этом году мы узнали, что если фаги и не очень живые, то уж точно очень общительные: находясь в разных клетках, они методично высылают друг другу сигналы — маленькие, но судьбоносные для фагов пептиды.
Бактериофаги (или просто фаги) — это вирусы, поражающие бактерий. После впрыскивания генома фага в клетку события могут развиваться по одному из двух сценариев:
литическому — когда фаг размножается, и армия новых его частиц бесцеремонно, нанося смертельные повреждения, покидает клетку;
лизогенному — когда геном фага встраивается в клеточную ДНК и остается до поры до времени в неактивном состоянии, подспудно защищая клетку от вторжения конкурентов — фагов своего вида.
В зависимости от условий бактериофаг выбирает, какой сценарий в данный момент для него выгоднее. Выбор пути регулируется чрезвычайно сложными механизмами. Заподозрить это позволяет даже количество работ, посвященных этой тематике: не одна сотня статей написана об одном только фаге λ и его выборе между лизисом и лизогенией. И всё равно система принятия решения осталась непонятой.
Зато с принятием решений у по-настоящему живых существ, бактерий, микробиологам более-менее удалось разобраться. Оказалось, что «примитивные одноклеточные» очень даже склонны к коллективному поведению. Им они эффективно пользуются в том числе и для того, чтобы причинить неприятности «высоколобым многоклеточным». Чувство кворума, или quorum sensing — механизм, используемый бактериями для передачи от клетки к клетке сигналов, которые чаще всего несут информацию о размере популяции и регулируют его. Грамположительные бактерии для этой цели предпочитают секретировать во внешнюю среду маленький пептид (часто менее 10 аминокислотных остатков), который при попадании в клетки других членов сообщества стимулирует специфические изменения экспрессии генов.
До сих пор quorum sensing считался прерогативой бактерий, и молекулярную коммуникацию между вирусами, находящимися в разных клетках, не обнаруживали.
Удивительная случайность (как всегда)
Израильская ученая Зохар Эрез с коллегами изучала бактерий, зараженных фагами группы SPbeta: пыталась обнаружить, секретируют ли Bacillus subtilis какие-либо молекулы, подготавливающие собратьев к фаговой атаке. Через три часа после заражения исследователи начали ловить в бактериальной культуре молекулы, которые могли бы предотвратить дальнейшую инфекцию. К своему удивлению они выделили белок не бактериального, а фагового происхождения. Этот маленький пептид синтезировал вирус phi3T, блокируя тем самым лизис клеток и стимулируя лизогению.
Эрез секвенировала геном бактериофага и идентифицировала ген, кодирующий нужный белок из 43-х аминокислотных остатков. Пептид получил название AimP. Он оказался поразительно похожим на сигнальные белки B. subtilis (в том числе вовлеченные в quorum sensing). Во время фаговой инфекции от синтезированного AimP ферментативно отрезался и секретировался во внешнюю среду пептид из шести аминокислот, который назвали арбитриумом (от лат. arbitrium — «решение»).
Бациллы обычно импортируют сигнальные пептиды в клетку с помощью олигопептидной пермеазы (OPP). Удалив ген одной из субъединиц OPP из генома бактерий (то есть «выключив» фермент), ученые установили, что арбитриум транспортируется в клетку именно таким путем. Чем больше фагового сигнального пептида поступало в клетку, тем выше была вероятность, что инфекция phi3T разовьется по лизогенному сценарию. При высоких концентрациях арбитриума лизис в культуре бацилл подавлялся окончательно (рис. 1).
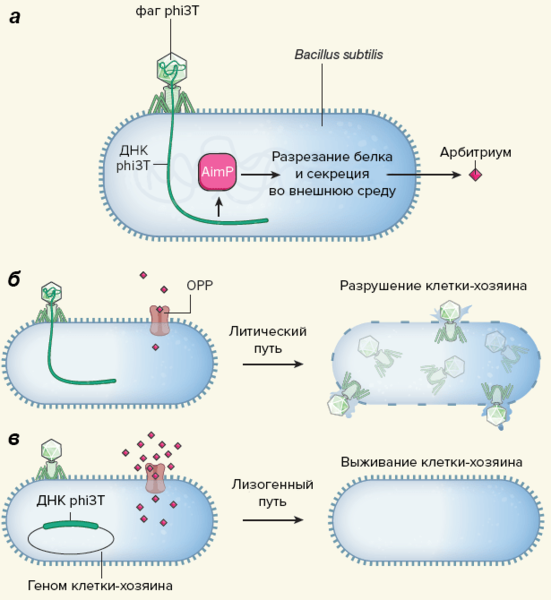
Рисунок 1. Фаги используют сигнальные пептиды для общения. а — После заражения бацилл фагом phi3T синтезируется вирусный белок AimP, от которого отрезается и секретируется из клетки маленький пептид арбитриум. б — Арбитриум попадает в другую клетку с помощью олигопептидной пермеазы, OPP. Если концентрация пептида мала, то развитие фага в этой клетке идет по литическому пути, и клетка разрушается. в — Высокая концентрация арбитриума способствует встраиванию вирусного генома в ДНК бациллы, клетка выживает, а другой phi3T уже не может ее инфицировать.
Белки фагового кворума и их гены
Вирус phi3T изолировали 40 лет назад и отнесли к группе SPbeta-фагов. Зохар Эрез впервые изучила его геном и выяснила, что при размере 128 т.п.н. он содержит 201 ген. Ген aimP кодирует белок AimP — так называемый пре-про-пептид, который в качестве «пре-» содержит N-концевую сигнальную последовательность, распознаваемую системой секреции и во время этой сáмой секреции отрезаемую (рис. 2). Вышедший наружу про-пептид обрабатывается бактериальной протеазой, лишаясь своей «про-». В результате остается зрелый короткий пептид из шести аминокислотных остатков, которые у про-пептида располагались на C-конце: Ser-Ala-Ile-Arg-Gly-Ala (SAIRGA).
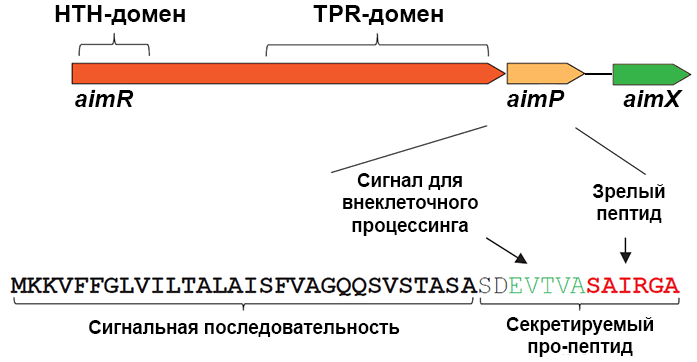
Рисунок 2. Гены кворума фага phi3T и структура белка AimP. Условные обозначения: HTH-домен — домен связывания с ДНК, TPR-домен — рецептор арбитриума.
Чтобы показать, что SAIRGA — это и есть арбитриум, израильские ученые заражали культуру бацилл фагом phi3T при высокой концентрации SAIRGA и наблюдали явное снижение числа лизированных клеток. Эффекта не было при проведении эксперимента с более короткими версиями пептида (SAIRG или AIRGA) и с бациллярным пептидом PhrC, участвующим в бактериальном кворуме.
Перед aimP в геноме фага расположен ген aimR, кодирующий белок длиной 378 а.о. Выяснили, что белок AimR — это внутриклеточный рецептор арбитриума: его С-концевой домен взаимодействует с сигнальной молекулой. В то же время N-концевой домен AimR приспособлен для специфического связывания с ДНК бактериофага (рис. 2).
После aimP находится ген aimX, который непосредственно участвует в выборе пути развития фага: его продукт длиной 51 а.о. каким-то образом активирует литический сценарий (рис. 2). На конце мРНК AimX находится добавочная некодирующая последовательность из 62 нуклеотидов, которая образует «шпильку» и, скорее всего, функционирует как регуляторная РНК.
Как работает система кворума бактериофагов?
На начальной стадии инфекции phi3T экспрессирует ранние гены — aimP и aimR. Белок AimR в виде гомодимера связывается со специфическим сайтом между aimP и aimX и активирует транскрипцию последнего (рис. 3а). В то время как новые порции AimP превращаются в арбитриум и выходят из клетки, AimX активирует литический цикл (а может, ингибирует лизогенный) — собираются фаговые частицы следующего поколения, разрушают клетку и заражают соседних бацилл.
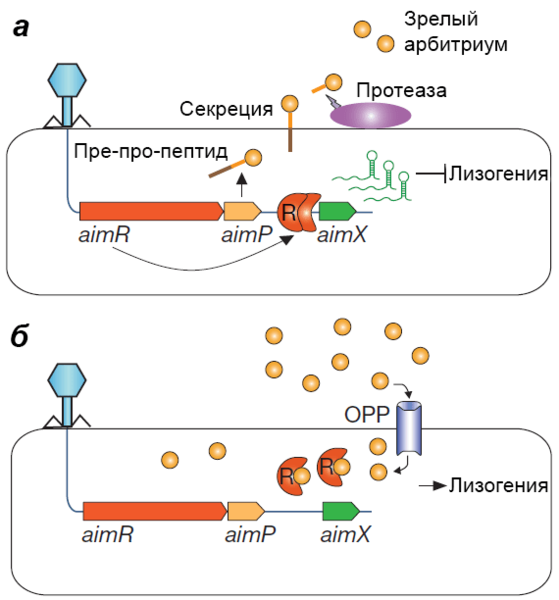
Рисунок 3. Модель работы системы quorum sensing фага phi3T. а — Развитие по литическому пути. б — Развитие по лизогенному пути. Подробные объяснения — в тексте.
Так происходит, пока в среде не создастся достаточно высокая концентрация арбитриума. В этом случае в инфицированные phi3T клетки через транспортер ОРР будет поступать настолько много сигнального пептида, что он сможет связаться со всеми рецепторными молекулами AimR, разбить димер на мономеры и тем самым помешать ему активировать транскрипцию aimX (рис. 3б).
Но зачем это нужно фагу? Логика проста. В начале фаговой атаки незараженных клеток очень много, а частиц фага мало — есть, где разгуляться. Поэтому вирусу незачем отсиживаться в клетке и бездействовать. Он активно размножается и инфицирует всё больше и больше бацилл. Наконец количество «свободных» клеток сокращается настолько, что это грозит полным уничтожением бактериальной популяции, а следовательно, и самих зарвавшихся паразитов. Именно о такой ситуации сообщает арбитриум (рис. 4). В результате вирусы «одумываются» — перестают размножаться и встраиваются в ДНК бактерий, чтобы дать возможность уцелевшим свободным клеткам нарастить популяцию. Позже цикл повторяется.
Рисунок 4. Демографическая ситуация — главный вопрос в беседах бактериофагов.
С обнаружением первой системы фаговой коммуникации пришло понимание того, что не только прокариоты, но и вирусы — не такие уж простачки. Геномы многих фагов еще не расшифрованы, и кто знает, какие новые сюрпризы преподнесут нам эти недоорганизмы? А что, если вирусы эукариот тоже общительны, и весь этот вирусный мир беседует не только о демографии?
Источник: БИОМОЛЕКУЛА

