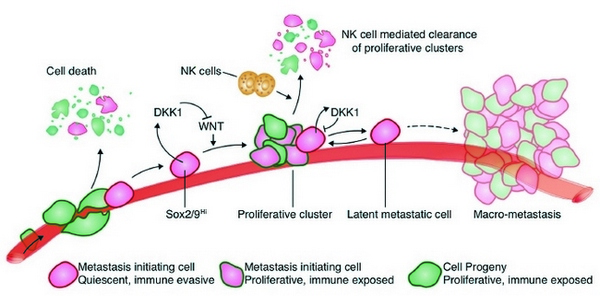
 Рис. 1. Основные события и механизмы отбора и поддержания раковых клеток в латентном состоянии. Большинство отделившихся от опухоли клеток, попадая в кровоток, разрушается под действием защитных механизмов, прежде всего вследствие атаки естественными киллерами (NK cells). Но клоны со свойственной стволовым клеткам усиленной экспрессией факторов транскрипции SOX2/SOX9 могут уклониться от действия иммунной системы и поселиться в различных органах. Если под влиянием факторов микроокружения такие латентные раковые клетки (LCC) начинают реплицироваться, то естественные киллеры предотвращают размножение их потомства, и сохраняются только «спящие» латентные раковые клетки. Вследствие усиленной экспрессии в латентных раковых клетках гена DDK1 в них подавлена активность сигнального пути WNT, активирующего пролиферацию. Кроме того, в латентных раковых клетках подавлена экспрессия лигандов, необходимых для узнавания их киллерами, и они уклоняются от элиминации естественными киллерами. Через какое-то время латентные раковые клетки могут «проснуться», начать реплицироваться и образовать метастазы.
Рис. 1. Основные события и механизмы отбора и поддержания раковых клеток в латентном состоянии. Большинство отделившихся от опухоли клеток, попадая в кровоток, разрушается под действием защитных механизмов, прежде всего вследствие атаки естественными киллерами (NK cells). Но клоны со свойственной стволовым клеткам усиленной экспрессией факторов транскрипции SOX2/SOX9 могут уклониться от действия иммунной системы и поселиться в различных органах. Если под влиянием факторов микроокружения такие латентные раковые клетки (LCC) начинают реплицироваться, то естественные киллеры предотвращают размножение их потомства, и сохраняются только «спящие» латентные раковые клетки. Вследствие усиленной экспрессии в латентных раковых клетках гена DDK1 в них подавлена активность сигнального пути WNT, активирующего пролиферацию. Кроме того, в латентных раковых клетках подавлена экспрессия лигандов, необходимых для узнавания их киллерами, и они уклоняются от элиминации естественными киллерами. Через какое-то время латентные раковые клетки могут «проснуться», начать реплицироваться и образовать метастазы.
Через несколько месяцев или лет после успешного удаления раковой опухоли, даже на ранних стадиях ее роста, могут развиться удаленные метастазы. Это серьезная проблема в лечении онкологических заболеваний. Недавно ученым удалось сделать шаг к ее решению: найдены клоны клеток рака легких и молочной железы человека, которые при инъекции подопытным мышам образуют опухоли очень нескоро — через несколько месяцев. Показано, что эти клетки «впадают в спячку» — переходят в латентное состояние — вследствие подавления индуктора пролиферации сигнального пути WNT. Также определены механизмы, позволяющие латентным клеткам уклоняться от иммунного ответа и активироваться при определенных условиях, чтобы дать начало новым опухолям.
Рак не перестает удивлять исследователей и врачей своим коварством. Казалось бы, опухоль у пациента аккуратно и своевременно удалена, метастазов в лимфатических узлах не найдено. Но через довольно длительное время, порой через несколько лет, у пациентов, у которых опухоль удаляли даже на ранних стадиях ее развития, возникают удаленные метастазы. В случае аденокарциномы легких это происходит у половины пациентов. Аналогичные события наблюдаются после поначалу успешной терапии рака молочной железы с помощью антител.
Источником этих осложнений являются свободные или диссеминирующие опухолевые клетки (disseminated tumor cells, DTCs). Некоторые из них обладают свойствами так называемых латентных раковых клеток (latency competent cancer cells, LCC cells). До того как был поставлен диагноз и удалена опухоль, из нее успевает отпочковаться множество свободных опухолевых клеток. Большинство их погибает в кровотоке или в органах, куда они были занесены. Но некоторые могут выжить и существовать в латентном состоянии в различных органах и тканях. Такие латентные метастазы представляют собой большую нерешенную проблему в клинической онкологии. Об их природе и механизмах, которые позволяют им оставаться в «спящем» состоянии, уклоняясь от действия систем иммунитета и сохраняя способность инициировать опухоли и превращаться в агрессивные метастазы, известно еще очень мало. Причиной этого, в частности, было отсутствие адекватных животных моделей, воспроизводящих ключевые свойства, механизмы формирования, существования и активации спящих метастазов.
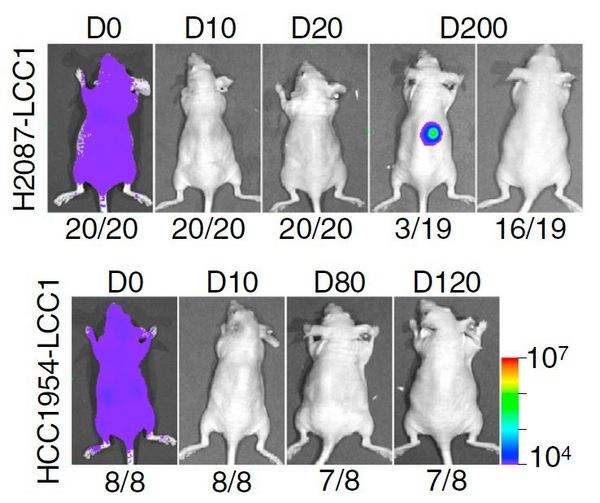
Рис. 2. Экспериментальные мыши после введения им двух различных клонов латентных раковых клеток (LCC). Изображения получены с помощью биолюминисцентного имиджера (см. bioluminescence imaging). D0–200 — дни наблюдения. Под изображениями — доля животных с изображенным имиджем.
Группа американских ученых разработала экспериментальные мышиные модели для исследования латентных метастазов. С помощью методов генетической инженерии они ввели в культивируемые клетки ранней аденокарциномы легкого H2087 или рака молочной железы человека HСС1954 гены зеленого флуоресцентного белка (GFP), люциферазы и устойчивости к антибиотику. Затем их вводили мышам, и из органов, в которых обнаруживались единичные GFP-положительные клетки, их клонировали и размножали в культуре. В результате были отобраны клоны клеток, которые при введении в кровоток мышей образовывали метастазы в различных органах только по прошествии нескольких месяцев (рис. 2) или в течение длительного времени не образовывали метастазы вообще и обнаруживались только гистологически (рис. 3). Эти клетки (H2087–LCC и HСС1954–LCC соответственно) проявляли свойства латентных метастазов. Они впадали в «спячку», пребывая в латентном состоянии в различных органах в течение месяцев и сохраняя способность затем давать метастазы.
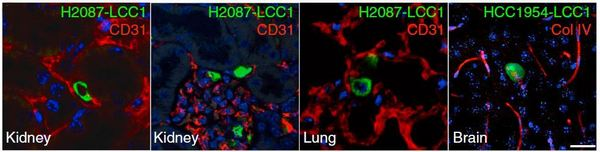
Рис. 3. Единичные латентные раковые клетки клетки (зеленые) в капиллярах и паренхиме различных органов: kidney — почка, lung — легкое, brain — мозг.
Далее авторы сравнили ряд молекулярных характеристик латентных раковых клеток и исходных культур H2087 и HСС1954. Оказалось, что наборы экспрессирующихся генов в латентных раковых клетках сильно отличались от таковых в исходных клетках и приобретали сходство с наборами генов, экспрессирующихся в стволовых клетках соответствующих тканей и в клетках, еще не прошедших полную дифференцировку. Известно, что специфическим свойством стволовых и недифферцированных клеток является усиленная экспрессия факторов регуляции транскрипции SOX2 и SOX9. Различными методами было показано значительное усиление экспрессии SOX2 в клетках H2087–LCC и SOX9 в HСС1954–LCC (рис. 4). Усиленная экспрессия этих факторов оказалась очень важной для заселения LCC-клетками различных органов в форме латентных метастазов. Подавление экспрессии SOX с помощью введения в клетки соответствующих анти-SOX shRNA резко подавляло их способность образовывать такие метастазы.
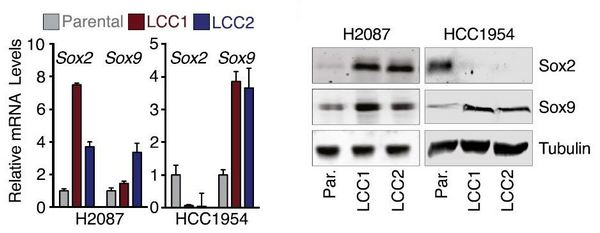
Рис. 4. Активация экспрессии транскрипционных факторов SOX2 и SOX9 в различных клонах латентных раковых клеток (LCC) на уровне мРНК (слева) и белка (справа). Parental — исходные клетки Н2087 и НСС1954, LCC1 и LCC2 — различные клоны латентных раковых клеток.
Организм может препятствовать распространению свободных опухолевых клеток и в том числе латентных раковых клеток различными способами. Наиболее эффективным из них представляется механизм врожденного иммунитета. Определенный класс лимфоцитов, названных естественными киллерами (natural killer cells, NK), способен атаковать и уничтожать чужеродные или аномальные клетки. Подавление активности естественных киллеров специфическими антителами активизировало рост метастазов, обусловленных «пробуждающимися» латентными раковыми клетками. Но естественные киллеры слабо действовали на латентные раковые клетки (рис. 5). Оказалось, что в латентных раковых клетках была сильно подавлена экспрессия ряда белков, необходимых для их узнавания и атаки киллерами.
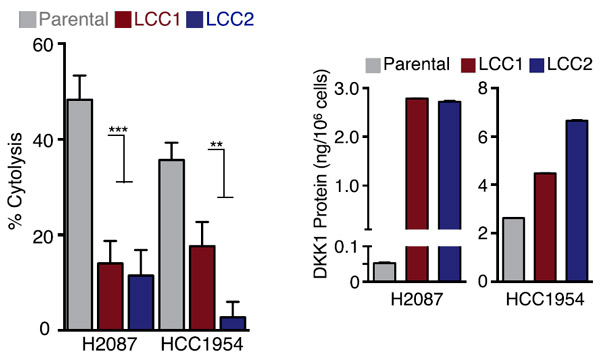
Рис. 5. Слева: лизис различных клеток in vitro под действием естественных киллеров (NK). Справа: усиление экспрессии гена DDK1 в латентных раковых клетках. Parental — исходные клетки Н2087 и НСС1954, LCC1 и LCC2 — различные клоны латентных раковых клеток.
С целью определения причин, по которым латентные раковые клетки сохраняли устойчивое к иммунитету латентное состояние, в них была исследована активность сигнальных путей. Наиболее заметным оказалось подавление сигнального пути WNT, который является сильным активатором деления стволовых и дифференцирующихся клеток. Представлялось логичным предположить, что в латентных раковых клетках экспрессируется какой-то ингибитор WNT. И действительно, оказалось, что в отличие от исходных клеток H2087 и HСС1954 в H2087–LCC и HСС1954–LCC усиленно экспрессируется ингибитор WNT DKK1. Известно, что ген DKK1 активируется фактором регуляции транскрипции SOX2. И эксперименты показали, что в H2087–LCC SOX2 связывается с промотором DKK1 и усиливает его экспрессию. А подавление экспрессии гена SOX2 с помощью shRNA приводит к подавлению экспрессии гена DKK1. Прямое подавление синтеза DKK1 в LCC с помощью shRNA приводило к усилению в них экспрессии активаторов взаимодействия с естественными киллерами.
Таким образом получается, что первопричиной перехода клеток в состояние латентных является активация экспрессии факторов регуляции транскрипции SOX и индуцированное ими усиление экспрессии гена DKK1. Это приводит к подавлению экспрессии активаторов естественных киллеров. Поэтому DKK1 требуется чтобы защитить латентные раковые клетки от киллеров. И действительно, подавление экспрессии DKK1 в культуре до инъекции клеток мышам с помощью shRNA резко уменьшало количество латентных раковых клеток в легких. Но если латентные раковые клетки уже заселились, подавление экспрессии гена DKK1 активировало рост метастазов.
Полученные результаты раскрывают молекулярные механизмы формирования латентных раковых клеток. Они могут иметь очевидное применение в клинической практике. Так, известно, что усиленная инфильтрация естественных киллеров ряда раковых опухолей коррелируется с благоприятным прогнозом течения заболевания. Это может объяснено тем, что естественные киллеры держат метастазы под контролем. Снижение активности естественных киллеров может служить предупреждением об опасности рецидива рака. Возможно, в будущем появится способ реактивации лигандов естественных киллеров в спящих латентных раковых клетках с целью их иммунологической элиминации. Но важно, чтобы этот способ не индуцировал пролиферацию латентных раковых клеток и переход их в состояние активно растущих метастазов.
Источник: ЭЛЕМЕНТЫ БОЛЬШОЙ НАУКИ

