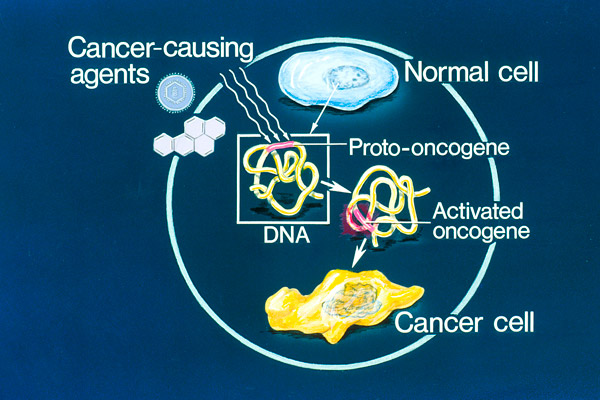
Рис. 1. Под действием канцерогена, ионизирующего излучения или спонтанной мутации протоонкоген может активироваться и превратиться в онкоген, индуцирующий рак.
Создание детального каталога раковых генов — важная задача, выполнение которой позволит подбирать оптимальную терапию онкологического заболевания для каждого пациента. Чтобы составить каталог раковых генов, мутирующих с высокой (>20%) и средней (2–20%) частотой, требуется проанализировать для каждого гена в среднем 2000 пар «опухоль — норма», то есть для 50 наиболее частых типов рака это примерно 100 000 пар. Сейчас это уже не является неразрешимой проблемой, так как за последние 10 лет стоимость секвенирования ДНК уменьшилась в миллион раз и будет уменьшаться еще.
В настоящее время рак занимает второе место среди причин смерти человека, уступая лишь сердечно-сосудистым заболеваниям (ежегодно в мире от рака умирает примерно 8 миллионов человек), а в некоторых развитых странах, например в Дании, рак уже вышел на первое место.
Рак — это сложное, динамически развивающееся заболевание, представленное более чем 200 известными типами и формами. Каждая из них требует индивидуального подхода, индивидуальной стратегии лечения. На генетическом уровне различные раки характеризуются различной «архитектурой» — наборами соматических мутаций, перестроек хромосом, а также эпигенетическими аномалиями, такими как изменение профиля метилирования генов. Следствием этих событий является изменение активности генов и(или) их продуктов.
Детальные сведения об аномалиях, связанных с возникновением и развитием раковых опухолей, требуются для диагностики и результативного лечения рака, для определения оптимальной терапии, а также для разработки новых противораковых средств. Объектами исследований являются аномалии молекулярной структуры ДНК, РНК, белков и эпигенетических аномалий (в частности, метилирования). Именно такой подход принят как генеральная стратегия, реализуемая несколькими национальными и международными консорциумами, которые объединяют десятки институтов, университетов и клиник. В работах участвуют сотни исследователей. Наибольшие успехи и наиболее ценные данные получены в результате поиска генов, связанных с инициацией, развитием и поддержанием злокачественной трансформации клеток.
Онкогены и антионкогены
В организме должен поддерживаться тонкий баланс между активностью генов и их продуктов, которые, с одной стороны, обеспечивают рост и деление клеток, а с другой стороны — предотвращают неограниченные рост и деление. Излишняя активность первых или подавление функции вторых приводят к неконтролируемому росту клеток, возникновению и развитию злокачественных неоплазий — раковых опухолей.
Связанные с раком гены можно разделить на два типа — онкогены и антионкогены (супрессоры опухолей), продукты которых могут, соответственно, стимулировать или подавлять образование и развитие опухолей. Особое место занимают микроРНК (miRNA) — короткие (в среднем ~22 нуклеотида) некодирующие РНК. К настоящему времени идентифицировано примерно 2000 различных микроРНК. Они способны подавлять трансляцию мРНК, считываемую с 30–60% генов человека. Некоторые микроРНК (oncomiR) способствуют злокачественной трансформации клеток, другие могут работать как антионкогены. В онкоген может превратиться нормальный ген — протоонкоген (рис. 1), который стимулирует рост клеток постоянно или на определенных стадиях развития организма. Трансформация протоонкогена в онкоген происходит в результате относительно незначительной модификации его естественной функции. Существуют следующие основные пути активации протоонкогена:
1) Мутация внутри протоонкогена или в его регуляторных элементах, которая меняет структуру белка и повышает активность кодируемого им белка (фермента) или усиливает экспрессию соответствующего гена.
2) Повышение концентрации белка из-за повышения его стабильности в клетке, увеличения периода полужизни и, соответственно, повышения активности.
3) Дупликация гена (увеличение количества копий), в результате чего повышается концентрация белка в клетке.
4) Транслокация гена, которая вызывает усиление его экспрессии или возникновение агрессивного гибридного гена.
Онкогенами являются, например, гены семейства Ras (сокр. от ‘Rat sarcoma’) — ГТФазы, участвующие в передаче сигналов, стимулирующих деление клеток.
Функция антионкогенов противоположна функции протоонкогенов. Антионкогены контролируют различные процессы, препятствующие злокачественной трансформации клеток:
1) Подавление избыточной экспрессии генов, обеспечивающих пролиферацию клеток.
2) Осуществление репарации ДНК (повреждения ДНК при подавлении репарации усиливают мутагенез и, как следствие, активацию протоонкогенов и инактивацию антионкогенов).
3) Координация пролиферации клеток с репарацией ДНК. Если репарация ДНК подавлена, они тормозят деление клетки и иницииируют апоптоз.
4) Контроль адгезии и механизмов контактного торможения делящихся клеток.
В общем, антионкогены ставят барьер неограниченному росту клеток. Утрата функции антионкогена разрушает этот барьер. Самым известным и часто мутирующим в раковых опухолях многих типов является антионкоген ТР53. Продукт ТР53 — фосфопротеин регулирующий транскрипцию ряда различных генов. В нормальной клетке он неактивен. При чрезвычайных событиях он активируется и выполняет роль «стража генома», осуществляя различные противораковые функции (рис. 2):
1) Активация системы репарации ДНК.
2) Если ДНК повреждена, ТР53 задерживает митоз делящихся клеток, блокируя переход из G1-фазы в S-фазу и предоставляя системе репарации время устранить повреждения.
3) Если устранить повреждения ДНК не удается, ТР53 включает программу гибели клеток — апоптоз.
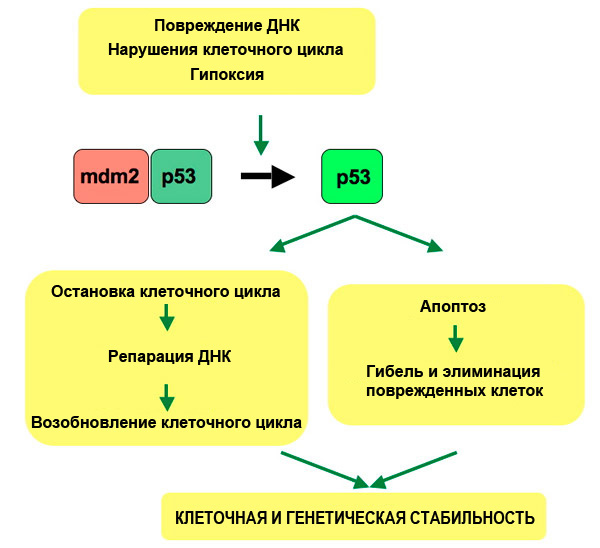
Рис. 2. В нормальных клетках р53 инактивирован негативным регулятором mdm2. При повреждениях ДНК или других стрессах комплекс р53-mdm2 распадается. Активированный р53 тормозит деление клетки до тех пор, пока поврежения не будут исправлены, или индуцирует программу апоптоза.
В случае, если рак вызван протоонкогеном, обычно достаточно активации этого протоонкогена на одной из двух парных клеточных хромосом. А вот если рак возник из-за утраты эффекта антионкогена, то, как правило, требуются мутации или потеря обеих его копий.
Сравнительное секвенирование
К настоящему времени идентифицировано примерно 300 онкогенов и супрессоров опухолей. Раковые гены ищут с помощью сравнительного секвенирования — то есть сравнивают последовательности нуклеотидов в ДНК опухолей и нормальных тканей и затем идентифицируют отсутствующие в ДНК нормальной ткани соматические мутации, которые встречаются чаще, чем просто случайные события.
Эта стратегия реализуется в несколько этапов. Во-первых, требуется получить образцы опухолевой ткани от пациентов с достоверно поставленным диагнозом и детально описанной картиной течения заболевания. При этом образцы должны быть, по возможности, свободны от нормальных клеток. Для сравнения используются пробы нормальной ткани или крови пациента. Из ткани опухоли и нормальной ткани выделяют ДНК и иссследуют их с помощью секвенирования. В последнее время секвенирование проводится с помощью платформ нового поколения, позволяющих быстро и сравнительно недорого полностью секвенировать геном человека. Результаты сравнительного секвенирования затем анализируются с помощью специально разработанных весьма сложных математических и биоинформатических методик.
Генеральной целью этих проектов является создание детального каталога аномалий структуры генома, связанных с инициацией, прогрессией и поддержанием онкологических новообразований. Такой каталог позволит не только получить много новых данных по молекулярной биологии рака, но и усовершенствовать методы диагностики, лечения и профилактики рака, определять новые мишени для разработки противораковых средств. Систематические исследования в этом направлении уже позволили идентифицировать много новых раковых генов и даже целые классы раковых генов.
«Атлас раковых геномов»
К настоящему времени уже проанализированы данные, полученные на больших выборках «опухоль — нормальная ткань» по более чем 30 формам рака. Наиболее заметных успехов добился реализуемый главным образом институтами и университетами США консорциум «Атлас раковых геномов» с многозначительной аббревиатурой TCGA — этими же буквами обозначают четыре нуклеотида, входящих в состав ДНК. Основанный в 2005 году, TCGA регулярно публикует в ведущих научных журналах результаты своих исследований. Рассказать обо всех публикациях консорциума здесь не представляется возможным. Приведем лишь результаты из последней статьи, посвященной плоскоклеточным ракам головы и шеи. Эта гетерогенная группа раков — шестая по частоте встречаемости и составляет ~5% всех случаев рака в мире.
В исследованиях участвовали 348 авторов. Было проанализировано 279 пар «опухоль — норма». Большинство опухолей, связанных с вирусами папилломы человека, имели мутации в спиральном домене онкогена PIK3CA. Обнаружены новые аномалии, включающие утрату TRAF3, амплификацию участвующего в контроле клеточного цикла гена E2F1. В опухолях, связанных с курением, почти всегда наблюдались инактивирующие мутации генов TP53 и CDKN2A, обнаруживались амплификации участков хромосом 3q26/28 и 11q13/22. Опухоли ротовой полости, сравнительно благоприятные с точки зрения возможности лечения и шансов на выздоровление, содержали активирующие мутации генов HRAS или PIK3CA в сочетании с инактивирующими мутациями генов CASP8, NOTCH1 и TP53. В случаях других подгрупп этого рака найдены инактивирующие мутации гена NSD1, продукт которого связан с перестройками хроматина, инактивирующие мутации генов AJUBA и FAT1, контролирующих ферменты сигнального пути Wnt, мутации, активирующие фактор оксидативного стресса NFE2L2.
«Умеренные» и «редкие» онкогены
Некоторые связанные с раком гены мутируют довольно часто — при многих или, по крайней мере, при нескольких типах рака. Поэтому неудивительно, что именно они (в частности, TP53) были охарактеризованы первыми. Но большинство раковых генов обнаруживаются с умеренной частотой (2–20%) или реже. Основные проблемы возникают при идентификации редких раковых генов. Так, недавнее исследование 183 аденокарцином легких показало, что у 15% пациентов не обнаруживается ни одной мутации в 10 известных для этого заболевания классах генов, а в 38% случаев идентифицировано три или менее мутаций.
Вследствие повреждения систем репарации ДНК в раковых клетках в той или иной мере усиливается мутагенез. Частота этих индуцированных опухолью соматических мутаций для различных опухолей может различаться на несколько порядков. Поэтому при идентификации «умеренных» и особенно «редких» генов возникает существенная проблема: как отличить гены и мутации, связанные с раком, от фона, от многочисленных случайных мутаций, не имеющих отношения к раку?
Гарвардская группа под руководством Г. Гетца разработала программный пакет MutSig (сокр. от ‘Mutation Significance’), анализирующий частоты и спектр мутаций в различных областях генома при различных формах рака, а также ряд других факторов, и позволяющий вычленить гены, достоверно мутирующие при раке (рис. 3).
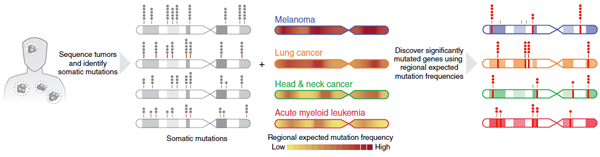
Рис. 3. Разные участки генома мутируют с различной частотой при различных формах рака. Алгоритм MutSig учитывает частоты и спектр мутаций, ряд других факторов, и позволяет найти гены, достоверно мутирующие при раке.
Мутации, достоверно связанные с раком
В двух статьях (M. S. Lawrence et al., 2013. Mutational heterogeneity in cancer and the search for new cancer-associated genes и M. S. Lawrence et al., 2014. Discovery and saturation analysis of cancer genes across 21 tumour types) авторы изучили собранные из различных баз данных результаты анализа экзомов (кодирующих областей генов — экзонов с прилежащими к ним последовательностями ДНК-некодирующих промежутков — интронов) 4742 пар «опухоль — нормальная ткань», принадлежащих к ракам 21 различных типов. Количество образцов для отдельных типов варьировало от 35 до 892.
Были обнаружены 3 078 483 единичные замены нуклеотидов в опухолях по сравнению с нормальной тканью, 77 270 единичных делеций или вставок нуклеотидов, 29 837 ди-, три- или олигонуклеотидных делеций или вставок. Из единичных замен нуклеотидов подавляющее большинство (2 294 935) не изменяло кодирующие последовательности. Из остальных единичных замен 540 831 представляли собой так называемые миссенс-мутации (приводящие к заменам аминокислот в белках), 207 144 представляли собой синонимические (не приводяшие к заменам аминокислот) замены нуклеотидов, 46 264 — нонсенс-мутации (приводящие к досрочной терминации синтеза белка), 33 673 — мутации, нарушающие сплайсинг мРНК (сборку кодирующих последовательностей мРНК из соответствующих блоков). Данные по «глубине» секвенирования и чистоте образцов опухолей позволяют оценить чувствительность анализа величиной больше 90% (рис. 4). Частоты возникновения мутаций на единицу длины генома для различных типов рака различались более чем на 5 порядков (от 0,03 до 7000 на миллион нуклеотидов ДНК), сильно различались и спектры мутаций.
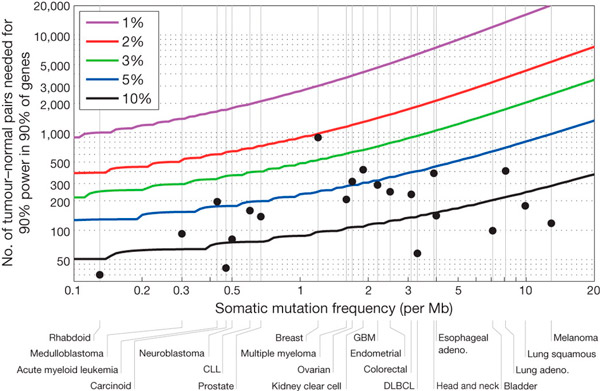
Рис. 4. Количество пар «опухоль — норма» (по оси ординат), необходимых для определения 90% генов, достоверно мутирующих при раке с вероятностью 90%. Оценки приведены в зависимости от типа опухоли, средней частоты фоновых мутаций (по оси абсцисс), превышения частоты мутаций раковых генов над фоном (цветные линии). Для большинства типов опухолей количество проанализированных проб еще недостаточно даже для того, чтобы детектировать гены, мутирующие с частотой над фоном 5% и менее. Черными точками показано количество уже проанализированных проб.
Мутации, достоверно связанные с раком, обнаруживались в 224 различных генах. Для различных типов рака число мутантных генов сильно варьировало (от 1 до 58). Для 7 типов оно было меньше 10, а для двух (раки молочной железы и эндометрия матки) — более 30. Только 22 гена оказались достоверно связанными с более чем тремя типами рака. Анализ позволил идентифицировать практически все ранее известные гены, связанные с канцерогенезом. Найдено также 33 гена, мутации в которых ранее не были проассоциированны с раком. Эти гены связаны с делением клеток, апоптозом, стабильностью генома, регуляцией активности хроматина, иммунным ответом, превращениями РНК и гомеостазом белков. Среди еще 81 гена также должны быть гены, связанные с раком.
На основании полученных результатов авторы произвели расчеты: сколько пар «опухоль — нормальная ткань» требуется проанализировать, чтобы найти достоверно мутирующие при раке гены в зависимости от типа рака, частоты мутаций на единицу длины генома при данном типе, частоты мутаций данного гена при данном типе рака. Расчеты показывают, что для 17 из 21 проанализированного типа рака данных еще недостаточно, чтобы выявить гены, мутирующие с частотой не выше 5% от фона. А для 7 типов — даже при частоте не выше 10%. Также определено, что для составления каталога раковых генов, перекрывающих 90% случаев заболевания, требуется проанализировать около 650 пар «опухоль — норма», если средняя частота мутаций составляет ~0,5 на миллион пар оснований ДНК (как при нейробластоме). Или даже около 5300 пар, если частота ~12,9 на миллион (как при меланоме). Всего же, чтобы для ~50 известных типов рака составить каталог соматических мутаций для генов, мутирующих с высокой (>20%) и средней (2–20%) частотой, требуется проанализировать в среднем 2000 пар «опухоль — норма», то есть всего примерно 100 000 пар.
В общем, создание детального каталога раковых генов — важная задача, выполнение которой позволит подбирать оптимальную терапию онкологического заболевания для каждого пациента: воздействия на определенные сигнальные пути или иные процессы, поврежденные в каждом конкретном случае. Такой каталог нужен также для выбора мишеней при разработке противораковых средств, создания новых экспериментальных моделей животных и линий клеток для исследования рака, испытания новых средств и методов лечения.
Источник: ЭЛЕМЕНТЫ БОЛЬШОЙ НАУКИ

